

| Home | HVAC | Zwembaden | Reiniging | Poort automatisering | Contact | Pers | Vacatures |
|---|
>32 jaar ingenieurservaring.
Het beste is maar goed genoeg.
GoLanTec energietechniek is een geregistreerd HVAC installatiebedrijf. Wij modificeren en bouwen €besparende en energiebesparende HVAC installaties.

Corrosie in de waterleiding is een probleem waar heel wat huizen te kampen hebben. Er komt roestwater uit de leidingen. Onder corrosie verstaat men de omzetting van metalen of legeringen naar oxides, hydroxides of zouten. Corrosie kan uiteindelijk leiden tot de vernieling van toestellen en installaties die met dit water in aanraking komen. Dit probleem kan snel en efficiënt opgelost worden via dosering van chemicaliën.
Corrosie
in sanitaire leidingen van gegalvaniseerd staal
In
sanitaire installaties worden nog steeds metalen leidingen toegepast. Deze
worden niet zelden aangetast door corrosie, tengevolge van foutieve beslissingen
met betrekking tot de opvatting van de constructie, de materiaalkeuze en het
gebruik of onderhoud van de installatie. In dit artikel zullen wij trachten een
overzicht te bieden van de meest voorkomende corrosiegevallen in sanitaire
installaties uit gegalvaniseerd staal.
1.
Inleiding
Stalen
leidingen kunnen enkel voor sanitaire toepassingen gebruikt worden indien deze
voorzien zijn van een zinklaag. Onbeschermd staal dat in contact komt met
zuurstofrijk water is immers heel snel onderhevig aan roest. Vermits zink de
ideale partner is in de strijd tegen staalcorrosie, werd in de Belgische norm
NBN EN
Met het oog op de vorming van de complexe beschermende patinalaag uit zinkoxides
en zinkhydroxides (pentazinkhydroxycarbonaat) op de interne buiswand, is de
samenstelling van het verdeelde water van primordiaal belang.
Indien zich bij de ingebruikname van de sanitaire installatie ongunstige
omstandigheden voordoen, zorgt het gevormde zinklaagje voor de kathodische
bescherming van het staal. Deze opofferingsbescherming komt tot stand doordat
het zink (onedel) gemakkelijker oxideerbaar is dan het staal (edel).
Aangezien dit mechanisme impliceert dat het zink gedeeltelijk opgelost wordt, is
het essentieel om deze kathodische bescherming in de tijd te beperken. Zoniet
zal het staal beginnen corroderen, waardoor het water rood zal kleuren.
In 2004 verscheen de Europese normenreeks EN 12502 inzake de bescherming van
metalen tegen corrosie, die sinds januari 2005 de status van een Belgische norm
heeft. Hierin worden de diverse corrosiefactoren (bv. de materiaaleigenschappen,
de waterkwaliteit, het ontwerp, de ingebruikname, het onderhoud en de werking
van de installatie), alsook de verschillende corrosievormen uit de doeken
gedaan.
2.
De meest voorkomende vormen van corrosie
2.1.
Corrosie tengevolge van de watersamenstelling
De
samenstelling van het verdeelde water moet in overeenstemming zijn met de
Europese Drinkwaterrichtlijn 98/83/EEG (L330).
Wanneer het verdeelde water in de binneninstallatie van het gebouw terechtkomt,
ondergaat dit een aantal fysische veranderingen (druk, temperatuur, …)
met mogelijke gevolgen voor de chemische samenstelling ervan. De waterkwaliteit
kan tevens wijzigen als gevolg van de eventuele waterbehandelingen (bv. waterverzachting).
2.2.
Corrosie die optreedt onder de afzettingslaag van vaste deeltjes
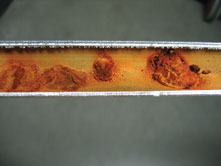
Afb.
1 Leiding uit
verzinkt staal met corrosie onder de afzettingslaag.
Het
binnendringen van vaste deeltjes (zand, klei, leem, …) in het leidingwater kan
een belangrijke invloed hebben op het ontstaan van een bepaald type corrosie. Zo
kan de hoeveelheid vaste partikels die in de installatie penetreren toenemen
door werken aan de hoofdleiding. Ook door de montage en de opslag van buizen in
een stofrijke omgeving, of door het binnendringen van ijzervijlsel bij het
versnijden ervan kunnen er vaste deeltjes in de installatie terechtkomen.
Deze vaste stoffen kunnen zich afzetten op de interne buiswand (en dan vooral op
de horizontale stukken), met zogenaamde corrosie door differentiële beluchting
of corrosie onder de afzettingslaag tot gevolg.
In dit geval vertoont de onderste buishelft plaatselijke corrosienodules,
wat kan leiden tot de doorboring van de buiswand. Het gaat hier niet om een algemene wanddiktevermindering, maar veeleer om een snelle,
gelokaliseerde perforatie (zie afbeelding 1).
2.3.
Corrosie door de vorming van een galvanisch koppel
Element
van Volta 
Het
primaire, elektrochemische corrosieverschijnsel is ontdekt door Alessandro
Volta, een Italiaans natuurkundige. Weliswaar was zijn voornaamste doel niet het
verklaren van corrosieverschijnselen, maar het doen van algemene natuurkundige
onderzoekingen, waaruit tenslotte een elektrische stroombron ontstond, het
element van Volta.
Dit
is de voorloper van onze batterij. Wat hij wel waarnam was, dat het onedele
metaal zink bij stroomlevering wordt aangetast en dat het meer edele metaal
koper, onveranderd blijft. (Bij het oplossen van zink in het element van Volta
komt de energie, die gebruikt is om het zink uit zijn erts vrij te maken, weer
tevoorschijn, nu in de vorm van elektrische energie). Een elektrochemische
corrosiecel ontstaat, wanneer twee verschillende metalen met elkaar in contact
zijn en wanneer een elektrolyt aanwezig is. Het minst edele van de twee metalen
gaat als primaire corrosiereactie elektrochemisch in oplossing, waarbij
elektriciteit wordt geleverd in de vorm van elektronen.
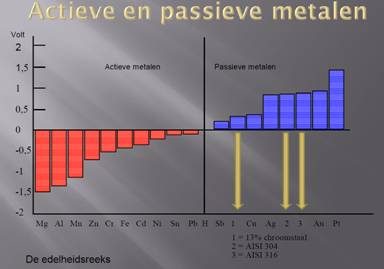
Zeer onedele metalen hebben een grotere oplosdruk dan minder edele metalen. Het is mogelijk deze oplosdruk te meten als een elektrische potentiaal. Als men nu de metalen rangschikt in volgorde van toenemende oplosdruk, krijgt men de spanningsreeks. Geheel onderaan staan de edele metalen, die een negatieve oplosdruk hebben, dan staat op plaats nul waterstof en daarboven staan de onedele metalen.
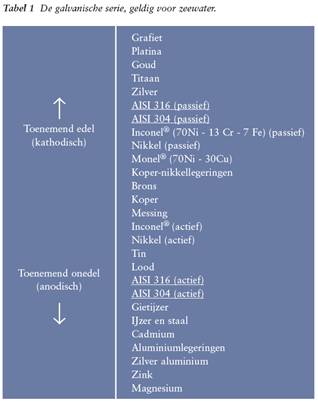
Elektrochemische spanningsreeks van de elementen. Elk metaal heeft een normaalpotentiaal (spanning) ten opzichte van waterstof. Plaatsen we de metalen in volgorde van oplopende potentiaalgrootte dan ontstaat de elektrochemische spanningsreeks van de elementen.
|
Na |
Mg |
Al |
Zn |
Cr |
Fe |
Sn |
Pb |
H |
Cu |
Ag |
Au |
|
-2,7V |
-2,4V |
-1,7V |
-0,76V |
-0,56V |
-0,44V |
-0,14V |
-0,12V |
0 |
+0,34V |
+0,8V |
+1,36V |
|
onedele metalen |
|
edele metalen |
|||||||||
2.3.1. Opgeloste koperionen
Bij koperen en zinken installaties moeten de koperen leidingen altijd stroomafwaarts van de verzinkte leidingen
worden geplaatst. De corrosie door de vorming van een 'galvanisch koppel' is
enkel reëel wanneer het water eerst het edeler metaal (koper) passeert en
daarna langs het minder edel metaal (zink) vloeit. Als er stroomopwaarts delen
in koper zijn, zal het leiding- of regenwater opgeloste koperionen
mee wegspoelen. Deze zetten zich stroomafwaarts in de leiding neer op het zink. Koper
is edeler dan zink en de zink onder het neergeslagen koper zal daardoor beginnen corroderen.
In
het geval van een dak gaat het over een geleidelijke afzetting en
geleidelijke aantasting. Hiervoor moet er zelfs geen constant contact zijn
tussen de twee metalen van de dakgoot. Als je buurman (in geval van een rijwoning
bijvoorbeeld) een koperen dakgoot heeft, waar het regenwater eerst over stroomt,
dan moet de erna komende afvoergoot minstens even edel is als de voorliggende
koperen dakgoot.
Er kan ook corrosie ontstaan door de aanwezigheid van opgeloste koperionen in een installatie met verzinkte leidingen. Daarom dient men er bij de uitvoering van gemengde sanitaire installaties (uit verzinkt staal en koper) over te waken dat het koper altijd stroomafwaarts van de galvanisé wordt geplaatst. De kans op corrosie door de vorming van een ‘galvanisch koppel’ is immers enkel reëel wanneer het water vanuit een leiding uit een edel materiaal (koper) in een leiding uit een minder edel materiaal (verzinkt staal) terechtkomt. Dit betekent dat het gebruik van koperen leidingstukken in een gesloten circuit met een retourleiding problematisch is. De plaatsing van een isolatiemof tussen het verzinkte staal en het koper zal voornoemde galvanische neerslagcorrosie niet verhelpen.
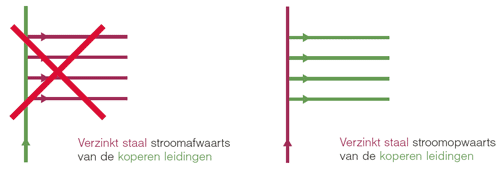
Afb.
2 Aanbevolen
plaatsing bij gebruik van koperen en gegalvaniseerde leidingen in eenzelfde
sanitaire installatie.
2.3.2. Contactcorrosie
Als koper en zink rechtstreeks met elkaar verbonden worden in leiding- of regenwater dan zal er heel veel corrosie zijn.
2.4.
Zwerfstroomcorrosie
Ook
stroombronnen (zoals slecht geïsoleerde elektrische installaties of
zwerfstromen, afkomstig van tram-, trein- of metrolijnen, …) kunnen aan de
bron liggen van de corrosie van de nabijgelegen metalen elementen. Dit
verschijnsel wordt aangeduid als ‘zwerfstroomcorrosie’.
Het gaat hier om een minder frequent voorkomende externe corrosievorm, die
aanleiding geeft tot plaatselijke putcorrosie.
2.5.
Corrosie als gevolg van potentiaalverschillen

Afb.
3 Externe corrosie
als gevolg van differentiële beluchting.
De
externe wanden van een metalen element kunnen aangetast worden door plaatselijke
corrosiecellen indien er potentiaalverschillen opgewekt worden door een verschil
van de zuurstofconcentratie (differentiële beluchting).
Zo kan de beschermende kleefband die rondom ingebouwde buizen aangebracht wordt
(bv. in muren of in een dekvloer) tijdens de droging een bescherming bieden
tegen corrosie. Dit materiaal vertoont evenwel slechts een beperkte mechanische
sterkte en is zeer kwetsbaar tijdens en na de plaatsing van de leidingen.
Indien er in een later stadium nog steeds vocht aanwezig is rondom de leiding,
kan er op de plaatsen waar de kleefband beschadigd werd corrosie ontstaan door
differentiële beluchting. Om deze reden moeten de leidingen, zelfs indien ze
voorzien werden van een bescherming, steeds bewaard worden in een droge
omgeving.
2.6.
Corrosie tengevolge van metallurgische factoren
Bij
de fabricage van metalen buizen worden verschillende behandelingstechnieken
gebruikt die tot bepaalde onvolkomenheden leiden waardoor het corrosieproces kan
bevorderd worden.
2.7.
Corrosie door micro-organismen
Een
minder gekende vorm van corrosie is deze, teweeggebracht door micro-organismen
(ook aangeduid als MIC of microbiologically influenced corrosion).
Het water, bestemd voor het drinkwaternet, moet normaalgesproken vrij zijn van
pathogene kiemen. Het aantal micro-organismen in de waterleiding kan echter
toenemen door nagroei op een geschikt substraat of door infecties via lekken.
Deze kiemen hechten zich vast op de wanden onder de vorm van een biofilm, waarin
ze gemakkelijk kunnen overleven en aangroeien. Een dergelijke biofilm kan niet
alleen verantwoordelijk zijn voor de verstopping van de leidingen en de
warmtewisselaar, maar kan tevens leiden tot de corrosie ervan.
3.
Preventieve en curatieve maatregelen
Corrosie
kan in bepaalde gevallen worden voorkomen door reeds van bij het ontwerp
rekening te houden met een aantal algemene aspecten (bv. de temperatuur, de
materiaalkeuze, …). Deze preventieve maatregelen zullen in detail besproken
worden in de lange versie van dit artikel. Toch is het zelfs met deze
maatregelen niet altijd mogelijk het risico op corrosieschade volledig uit te
sluiten.
Zo zal men soms genoodzaakt zijn om over te gaan tot een chemische behandeling
met inhibitoren. De fosfaatinjectie voor sanitaire toepassingen, die gebaseerd
is op de vorming van een beschermende film op het metaaloppervlak, is in deze
context genoegzaam bekend.
Voor andere, kleinere onderdelen van de installatie (bv. moeilijk toegankelijke
buisdelen), kan het mogelijk zijn om plaatselijk een organische coating (b.v.
epoxy) in de buizen aan te brengen.
4.
Besluit
HET IS NIET SIMPEL. Zie volgende zinsconstructie door WTCB:
Gelet op de complexiteit van de corrosieproblematiek in sanitaire leidingen van gegalvaniseerd staal en de talloze parameters die hierbij in rekening moeten gebracht worden, is het niet verwonderlijk dat elk afzonderlijk corrosiegeval een oordeelkundig onderzoek vereist, met het oog op het vergaren van de informatie die nodig is voor de opvatting, het goede gebruik en het onderhoud van de installatie.
Mooi gezegd!!!!!
 Perfecte
technologie, daar komt het op aan
Perfecte
technologie, daar komt het op aan
Versie laatst bewerkt op 20/11/2018